морфология
На макроскопическом уровне при болезни Альцгеймера можно наблюдать переменную степень кортикальной атрофии (уменьшение массы ткани или органа), характеризующейся расширением теменных борозд, более выраженных в лобных, височных и теменных долях. Эта атрофия компенсируется расширением желудочковых полостей, вторичным по отношению к потере паренхимы (рисунок 1). В частности, на поздних стадиях заболевания структуры медиальной височной доли, включая гиппокамп, энторинальную кору и миндалину, сильно атрофируются, учитывая их вовлечение, начиная с ранних стадий патологии.
Кроме того, болезнь Альцгеймера также представляет микроскопические изменения, известные как внеклеточные сенильные бляшки и внутриклеточные нейрофибриллярные кластеры, которые представляют собой основу гистологического диагноза. Таким образом, с прогрессированием заболевания происходит серьезная потеря нейронов, сопровождаемая глиозом (ограниченная или диффузная пролиферация, реактивная по природе, клеток нейроглии, то есть клеток, которые составляют поддерживающую строму нервной ткани) в тех же областях. где присутствие нейрофибриллярных бляшек и скоплений больше.
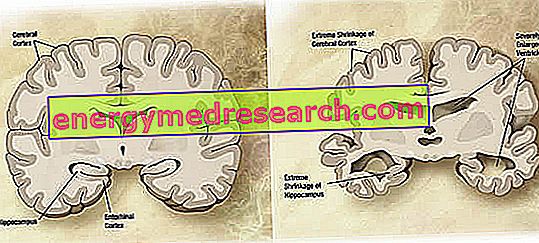
Рисунок 1. Корональный отдел головного мозга: различия между нормальным мозгом и мозгом, пораженным БА (источник изображения из Википедии).
патогенез
Болезнь Альцгеймера характеризуется в основном двумя типичными поражениями: внеклеточным накоплением сенильных бляшек, состоящих в основном из β-амилоидного пептида (Aβ) и внутринейрональных нейрофибриллярных кластеров, образованных гиперфосфорилированным тау-белком.
- Сенильные бляшки можно обнаружить на уровне областей мозга, таких как гиппокамп, миндалина и неокортекс.
Пептид Aβ происходит из протеолитического среза предшественника амилоидного белка (APP) посредством β-секретазы. Этот разрез генерирует концевой карбоксильный фрагмент из 99 остатков (CTF или C99), который впоследствии разрезается β-секретазой с образованием фрагментов Aβ, имеющих различную длину. Известно, что наиболее распространенным видом Aβ является фрагмент Aβ40. Другой известный фрагмент, образованный из протеолитического среза, менее распространенный, чем Aβ40, представляет собой Aβ42, более склонный к образованию амилоидных фибрилл, которые накапливаются в виде видов Aβ в головном мозге человека с болезнью Альцгеймера.
- Другой компонент, присутствующий при болезни Альцгеймера, представлен нейрофибриллярными кластерами, состоящими из пучков нитей, присутствующих в цитоплазме нейронов. Нейрофибриллярные кластеры нерастворимы и, по-видимому, устойчивы к процессам протеолиза in vivo, таким образом оставаясь в срезах тканей даже в течение длительного времени после гибели нейронов. Наблюдая за структурой, фибриллярные кластеры состоят из нитей с двойной спиралью и линейных нитей аналогичного состава. Анализируя состав, нити с двойной спиралью в основном состоят из гиперфосфорилированного тау-белка. Тау - это аксонный белок, связанный с микротрубочками, который облегчает его сборку.
Другие важные нейропатологические изменения, присутствующие при болезни Альцгеймера, включают митохондриальную дисфункцию, окислительное повреждение нейронов, синаптическую потерю и дегенерацию аксонов.
Нейрохимические аспекты
Как уже объяснялось, пептид Аβ, происходящий из протеолитического среза предшественника АРР, представляет нейротоксический компонент болезни Альцгеймера . В частности, было выдвинуто предположение, что Aβ может быть важным для нормальных функций мозга и, если он преодолевает определенные концентрации, он может стать нейротоксичным. Кроме того, как агрегаты, так и разные изоформы Aβ могут играть разную биологическую, физиологическую или патологическую роль, определяя и участвуя в последующих стадиях заболевания. Наблюдалось, что Aβ действует как нейромодулятор, влияя на высвобождение некоторых нейротрансмиттеров при отсутствии явных признаков нейротоксичности.
Например, нейромодулирующая роль Aβ в физиологическом контексте может иметь важное значение для правильного баланса нейротрансмиттерной системы. Хорошо известно, что эта система состоит из нейротрансмиттеров, веществ, которые передают информацию между клетками, составляющими нервную систему, нейронами, через синаптическую передачу.
В патологических условиях, с другой стороны, Aβ-опосредованная синаптическая передача может быть связана с изменением нейротрансмиссии перед нейродегенеративными событиями. В результате этих изменений могут возникать ранние когнитивные и некогнитивные расстройства на основе пораженных нейротрансмиттерных систем и различных участков мозга.
Изменения нейромедиаторных систем и механизма передачи сигнала в мозге людей, страдающих болезнью Альцгеймера, очень сложны. Одна из систем, которая, по-видимому, изменена, касается холинергической сигнальной системы, которая включает нейротрансмиттер ацетилхолин. Действительно, было показано, что у людей, страдающих болезнью Альцгеймера, наблюдается снижение холинергической передачи на уровне коры и гиппокампа, важных областей мозга, посвященных таким явлениям, как обучение и память. В дополнение к этой нейротрансмиттерной системе при болезни Альцгеймера наблюдались изменения в норадренергической, серотонинергической, а также глутаматной и ГАМК-системах.



