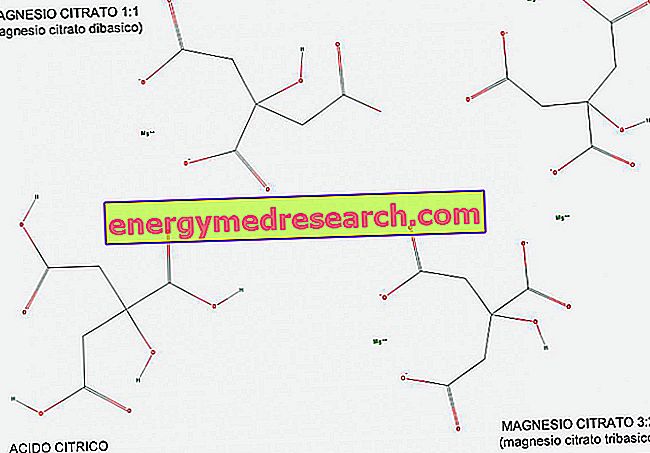
Трехосновная (или трипротонная) кислота представляет собой кислоту, которая имеет три иона водорода для донорства в кислотно-щелочной реакции. С помощью рисунка мы можем видеть, как лимонная кислота является примером трехосновной кислоты, поскольку она имеет три СООН-карбоксильные группы, которые могут легко переносить водород Н.
Цитрат магния существует как в пропорции 1: 1 (1 молекула магния на молекулу цитрата), так и в пропорции 3: 2 (3 молекулы магния на 2 молекулы цитрата).
Цитрат магния 1: 1 называют двухосновным, поскольку он представляет собой двухосновную соль лимонной кислоты; на самом деле он имеет 2 одновалентные основные группы (COO-) на молекулу, полученные из 2 карбоновых групп, которые в ходе реакции отказались от своего водорода.
Магний 3: 2, с другой стороны, называется трехосновным, потому что он имеет 3 одновалентные основные группы (COO-) на молекулу, полученные из 3 карбоновых групп, которые в ходе реакции выделяли водород.
Трехосновный цитрат магния явно богаче магнием (+ 42, 6% по массе), чем двухосновный цитрат магния; более того, он более подщелачивающий, так как он может принять три иона водорода Н + против двух, принятых двухосновным. Однако он менее растворим в воде.



